(2014秋•福建校级期中)将某质量的镁铝合金溶解在500mL盐酸中,向反应后的溶液中逐滴加入2mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示.请填写下列空白:https://bgk-photo.cdn.bcebos.com/doc/pic/item/0df431adcbef7609a6f7d3f326dda3cc7dd99eda.jpg(1)写出BC段发生反应的化学方程式:______.(2)合金中铝的质量为______.(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是______.
(2014秋•福建校级期中)将某质量的镁铝合金溶解在500mL盐酸中,向反应后的溶液中逐滴加入2mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示.请填写下列空白:https://bgk-photo.cdn.bcebos.com/doc/pic/item/0df431adcbef7609a6f7d3f326dda3cc7dd99eda.jpg(1)写出BC段发生反应的化学方程式:______.(2)合金中铝的质量为______.(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是______.
发布时间:2025-02-22 14:51:41
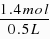 =2.8mol/L,故答案为:2.8mol/L.
=2.8mol/L,故答案为:2.8mol/L.

