简要解答下列问题。(1)氧元素的氢化物(H2O)在乙醇中的溶解度大于H2S,其原因是_________________。(2)已知苯酚(https://bgk-photo.cdn.bcebos.com/b90e7bec54e736d14541be698b504fc2d5626904.jpg)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子https://bgk-photo.cdn.bcebos.com/7aec54e736d12f2ed2579c015fc2d56285356804.jpg能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________(填“>”或“<”)Ka(苯酚),其原因是_______________________________。(3)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为_______________。https://bgk-photo.cdn.bcebos.com/4ec2d5628535e5dd967e97be66c6a7efce1b6204.jpg的沸点比https://bgk-photo.cdn.bcebos.com/f703738da9773912429bb700e8198618367ae216.jpg高,原因是____________________。
简要解答下列问题。(1)氧元素的氢化物(H2O)在乙醇中的溶解度大于H2S,其原因是_________________。(2)已知苯酚(https://bgk-photo.cdn.bcebos.com/b90e7bec54e736d14541be698b504fc2d5626904.jpg)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子https://bgk-photo.cdn.bcebos.com/7aec54e736d12f2ed2579c015fc2d56285356804.jpg能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________(填“>”或“<”)Ka(苯酚),其原因是_______________________________。(3)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为_______________。https://bgk-photo.cdn.bcebos.com/4ec2d5628535e5dd967e97be66c6a7efce1b6204.jpg的沸点比https://bgk-photo.cdn.bcebos.com/f703738da9773912429bb700e8198618367ae216.jpg高,原因是____________________。
发布时间:2025-03-30 18:31:14
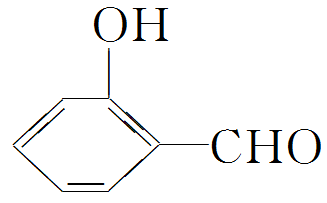 形成分子内氢键,而
形成分子内氢键,而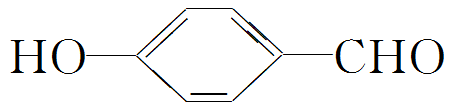 形成分子间氢键,分子间氢键使分子间作用力增大解析 (1)H2O在乙醇中的溶解度大于H2S,是因为水分子与乙醇分子之间可形成氢键。(2)氧的电负性较大,则
形成分子间氢键,分子间氢键使分子间作用力增大解析 (1)H2O在乙醇中的溶解度大于H2S,是因为水分子与乙醇分子之间可形成氢键。(2)氧的电负性较大,则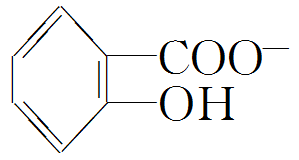 能形成分子内氢 键,即O—H…O(—COO-中双键氧与羟基氢之间存在氢键),其大小介于化学键和范德华力之间,使其更难电离出H+,则水杨酸第二级电离常数小于苯酚的电离常数。(3)氢键弱于共价键而强于范德华力。对羟基苯甲醛形成分子间氢键,使其沸点升高,邻羟基苯甲醛形成分子内氢键,对其沸点的影响不如分子间氢键。
能形成分子内氢 键,即O—H…O(—COO-中双键氧与羟基氢之间存在氢键),其大小介于化学键和范德华力之间,使其更难电离出H+,则水杨酸第二级电离常数小于苯酚的电离常数。(3)氢键弱于共价键而强于范德华力。对羟基苯甲醛形成分子间氢键,使其沸点升高,邻羟基苯甲醛形成分子内氢键,对其沸点的影响不如分子间氢键。

